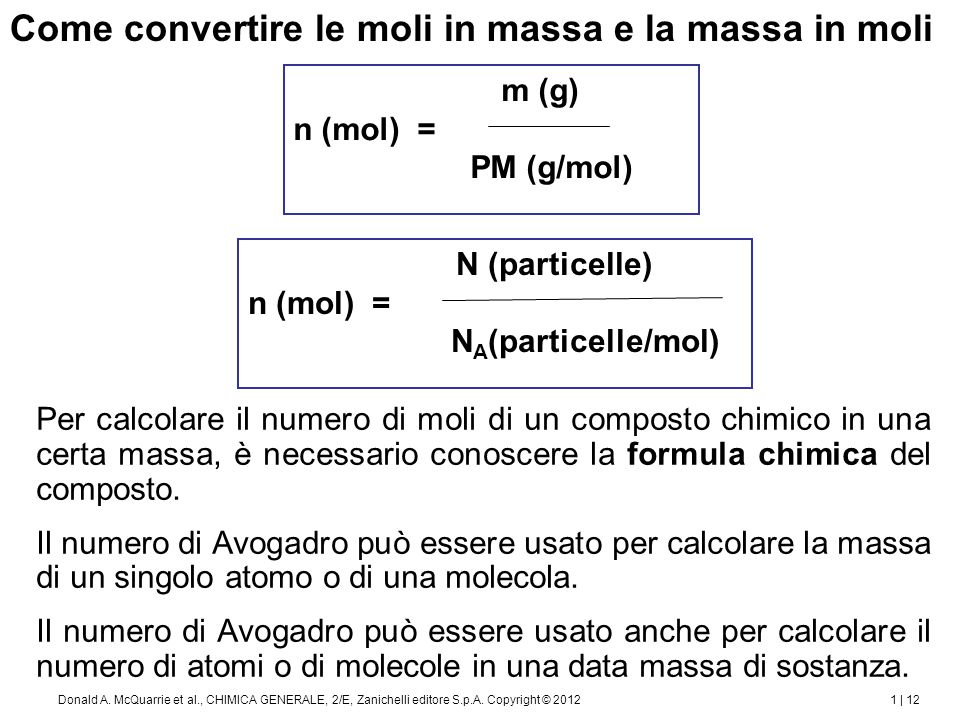
Il concetto di mole Quando due sostanze reagiscono tra di loro, dobbiamo poter prevedere: la massa di un composto che può essere preparata da una quantità. - ppt scaricare

Come possiamo conoscere il numero di atomi o molecole presenti in una definita quantità di sostanza? - ppt scaricare

Come possiamo conoscere il numero di atomi o molecole presenti in una definita quantità di sostanza? - ppt scaricare

MASSE ATOMICHE Difficoltà legate alla conoscenza della formula molecolare. Se l'acqua fosse HO avremmo la massa dell'ossigeno pari a 7,9367 g. Inizialmente. - ppt scaricare

Esercitazione 1 - MASSA ATOMICA, MASSA MOLECOLARE, MOLE. COMPOSIZIONE PERCENTUALE, FORMULA MINIMA. m - Studocu